
单臂试验和随机对照试验都可以帮助药物加速批准上市
日前,FDA肿瘤药物咨询委员会(ODAC)关上了抗肿瘤药物PI3K抑制剂通过单臂试验上市批准的大门,并且建议此类药物需用随机对照数据来支持。单臂试验一度做为PI3K抑制剂药物获批上市的捷径,但FDA此次的态度却发生了反转。
因为此前没有对抗肿瘤药物PI3K抑制剂的疗效剂量毒性关系进行仔细评估,所以FDA建议使用随机对照临床试验来降低安全问题。FDA同时表明,加速批准途径并不等同于单臂试验,随机对照试验可以为早期疗效终点和后期无进展生存期终点提供动力,从而使药品加速获批。
这表明单臂试验和随机对照试验都可以帮助药物加速批准上市。
单臂试验的优点
2014年,美国FDA批准了基于单臂数据的第一个抗肿瘤药物PI3K抑制剂idelalisib(Zydelig)的上市,我国2020年12月颁布《单臂试验支持上市的抗肿瘤药进入关键试验前临床方面沟通交流技术指导原则》后,依靠单臂试验上市成功的抗肿瘤药物也随之增多。随机对照试验(RCT)是目前国际上公认的证据级别最高的临床研究证据,是评价干预措施效果的金标准,多中心、双盲、随机临床试验是临床研究的主流,但非RCT试验单臂试验(SAT)不需随机、更无对照,相对于复杂的双盲随机对照试验,药企均期望以早期单臂试验数据来支持新药注册。
单臂试验的优点有:
1.减少样本量,可以是单中心;
2.疗效评价用时短;
3.显著缩短临床研发时间。
据报道,FDA批准的抗肿瘤新药使用SAT相比随机对照试验将临床研发时间缩短了2年。相关文献分析,FDA加速批准的基于单臂试验的药物其治疗效果适中,偏倚风险高。
FDA批准通过单臂试验上市的理由和指导文件:
1. FDA《Expedited Programs for Serious Conditions——Drugs and Biologics》针对严重疾病的药物和生物制品加速审批计划指出,“某些癌症类型中肿瘤缩小(反应率)的放射影像学证据被认为可以合理地预测总体生存期的改善”作为加速批准(AA)计划批准的示例。
2. FDA《Clinical Trial Endpoints for the Approval of Cancer Drugs andBiologics》针对癌症药物和生物制品批准的临床试验终点指出,“FDA有时接受客观缓解率(ORR)和在单臂试验中观察到的反应持续时间作为支持加速批准的实质性证据。”因此,ORR的大小很重要,一般来说,决策是基于高ORR。由于新药预期具有临床意义的ORR大小因癌症类型和治疗而异,因此批准所需的ORR大小因每个适应症而异。
FDA批准通过单臂试验上市的药物涵盖抗体偶联物、激酶抑制剂、免疫检查点抑制剂、靶向药物、CAR-T细胞药物、光学显像剂、重组酶、双特异性抗体、抗癌肽药物偶联物、化疗等,这些药物主要用于治疗癌症。在FDA官网查询药物批准公告,自2021年1月至2022年4月26日,批准的67个新药中通过单臂试验上市的药物共24个(具体见下表),占比35.82%。

单臂试验获批药物适应症主要为癌症
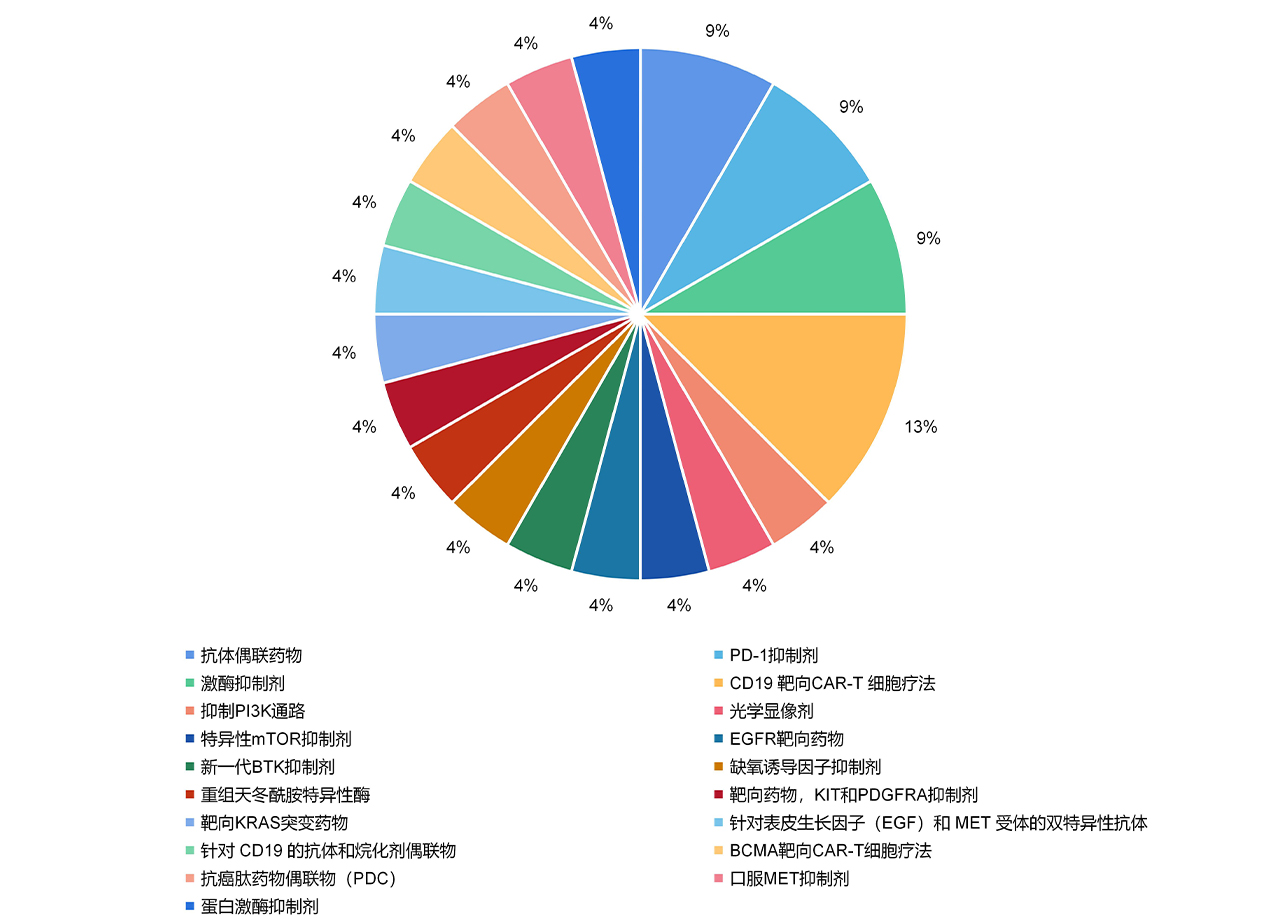
单臂试验获批药物的作用机制不断创新
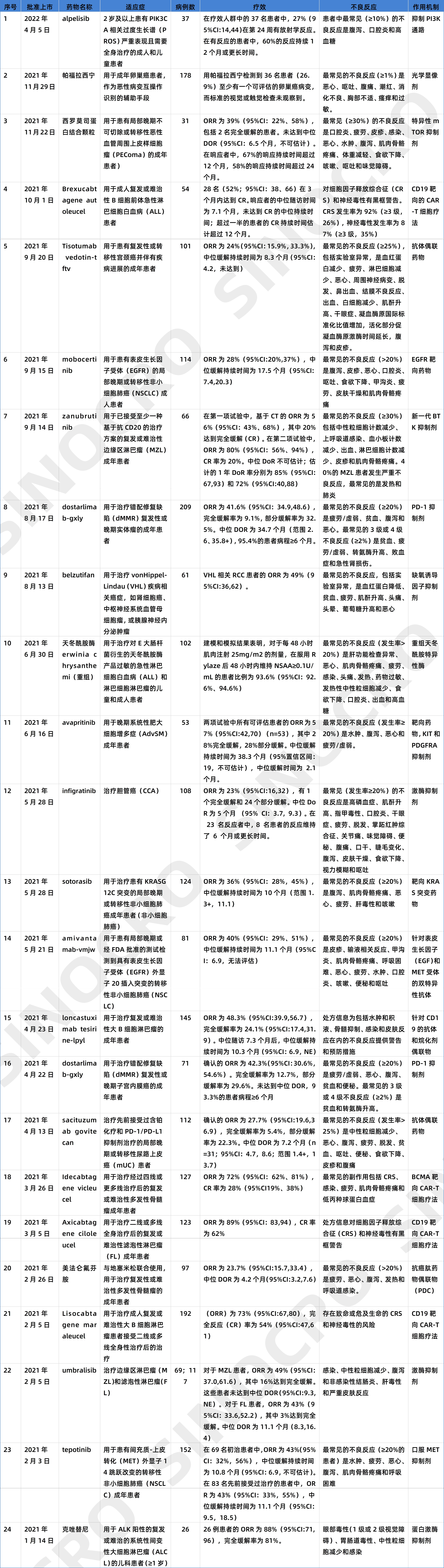
FDA最近批准通过单臂试验获批上市的药品案例以及相关考量
2022年4月5日,FDA加速批准alpelisib用于2岁及以上患有PIK3CA相关过度生长谱(PROS)严重表现且需要全身治疗的成人和儿童患者。使用来自真实世界数据评估疗效,采用单臂临床研究,主要疗效结果测量是由盲法独立中央放射学审查确定的第24周放射学反应患者的比例,定义为在多达3个病灶中确认的可测量靶病灶体积之和从基线减少≥20%至少1次后续影像学评估。反应持续时间是一项额外的疗效结果测量。在疗效人群中的37名患者中,27%(95%CI:14,44)在第24周有放射学反应。在有反应的患者中,60%的反应持续12个月或更长时间。
PIK3CA相关的过度生长谱(PROS)是一组罕见的疾病。FDA该项审查使用了实时肿瘤审查(RTOR)试点计划,该计划在提交整个临床申请之前简化了数据提交以及评估援助,以促进FDA的评估。此外,FDA基于对严重疾病的加速审批文件,对该药进行了优先审评、突破性认定和孤儿药认定。
单臂试验和双盲随机对照试验的优劣势与适用范围
一、单臂试验的优劣势与适用范围:
单臂试验的优势:
1.减少样本量,可以是单中心;
2.疗效评价用时短;
3.显著缩短临床研发时间。
单臂试验的劣势:
1.临床试验中的混杂因素难以控制;
2.结果的可预见性难以确定;
3.卫生技术评估(HTA)对单臂试验的可接受程度还存在质疑。
单臂试验的适用范围:
1.对罕见病或超罕见病的孤儿药评价,采用RCT方法不可行,而且有悖于伦理问题;
2.一些具有突破性的治疗方法为加速审批、快速招募患者,不可能开展RCT研究;
3.针对高度未满足的医疗需求;
4.患者人数极少,疾病自然史很清楚,研究药物与已有的标准疗法(SOC)相比具有很明显的效果;
5.可采用历史性数据或真实世界数据来对照比较分析。
二、双盲随机对照试验的优劣势与适用范围
优势:
1.可以在随机对照试验(RCT)的多个阶段控制偏倚;
2.可以减少对结局事件的差异性评估。
劣势:
1.并不是所有研究都能够做成双盲,特别是外科手术或开放性的试验。
2.若分配隐藏不充分,将会破坏盲法。
双盲随机对照试验的适用范围:
1.适用于容易找到足够多标准样本的实验;
2.适用于病程较长的轻、中症疾病,此外重症医学领域由于研究场所和患者的特殊性,小样本量的RCT较为常见。
全球双盲试验数量庞大:
从clinicaltrials官网查询,全球共有42258项双盲试验,其中已完成的有26858项,完成有结果的有10512项,在招募状态中的有4577项,撤销的有1180项。
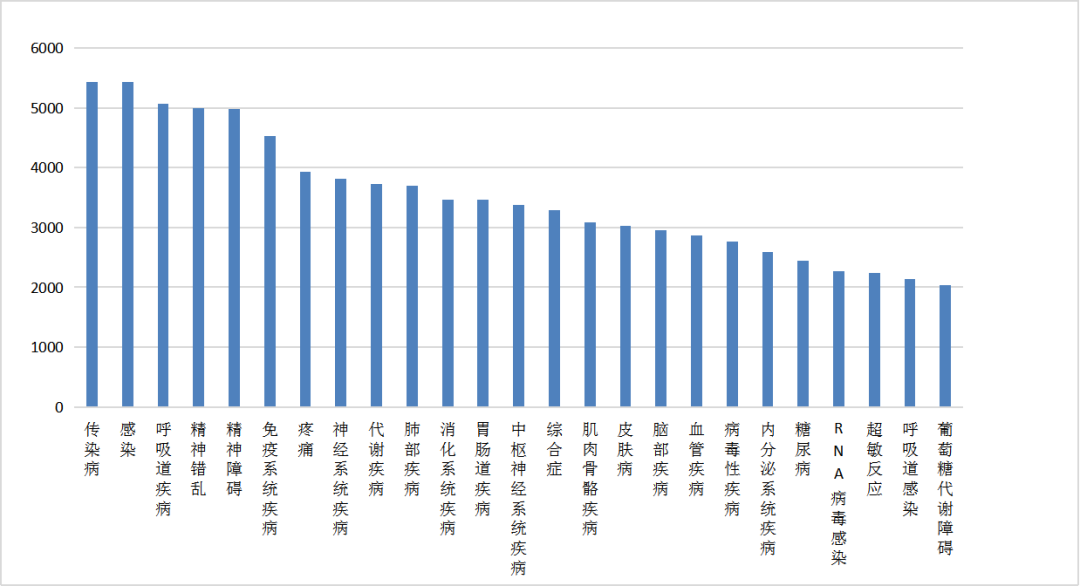
图为全球双盲试验涉及疾病领域(前25个领域)
不感兴趣
看过了
取消

人点赞

人收藏

打赏
不感兴趣
看过了
取消






您已认证成功,可享专属会员优惠,买1年送3个月!
开通会员,资料、课程、直播、报告等海量内容免费看!

打赏金额
认可我就打赏我~
1元 5元 10元 20元 50元 其它
打赏作者
认可我就打赏我~
扫描二维码
立即打赏给Ta吧!
温馨提示:仅支持微信支付!
已收到您的咨询诉求 我们会尽快联系您
