几十年来,应激和肿瘤之间相互关联的观点一直主导着外行的讨论。最近的动物研究结果表明,应激可以通过调节肿瘤的大多数特征来促进癌症的进展,并且介导这些作用的分子和系统机制已经被阐明。
几十年来,应激和肿瘤之间相互关联的观点一直主导着外行的讨论。最近的动物研究结果表明,应激可以通过调节肿瘤的大多数特征来促进癌症的进展,并且介导这些作用的分子和系统机制已经被阐明。然而,关于这种有害作用的现有临床证据是不一致的,因为流行病学和减轻应激的临床干预对肿瘤的死亡率产生了不同的影响。2021年9月10日,来自以色列特拉维夫大学萨戈尔神经科学学院和心理科学学院的Shamgar Ben-Eliyahu教授课题组在《Nat Rev Cancer》(IF: 60.7)杂志上发表题为《Stress and cancer: mechanisms, significance and future directions》的综述,旨在介绍和讨论临床前研究的具体介导机制,解释临床前和临床结果之间的差异、阐明应激影响肿瘤的机制以及肿瘤患者的应激管理等,现介绍如下:
研究背景
几十年来,人们一直认为应激会影响肿瘤的发病率和进展。然而,流行病学研究和临床研究却显示出不一样的结果,或研究表明应激对肿瘤进展的影响很小或不显著。因此,目前的医疗没有将控制应激反应的措施作为提高癌症存活率的常规手段。这导致医学界对应激是癌症病因和进展的一个重要的生物学因素这一观点仍持有怀疑态度。相比之下,近年来,动物研究提供了确凿的证据,表明应激可以促进多种癌症的生长和转移。最重要的是,这些效应背后的许多内分泌、细胞和分子机制已经被确定。例如,动物实验结果表明,应激可以通过直接促进肿瘤的恶性特征、重塑肿瘤微环境、削弱机体的抗肿瘤免疫反应来促进肿瘤进展与转移。在这篇综述中,作者阐述了机体水平以及肿瘤背景下的应激与应激反应;并且基于动物研究和临床研究的结果,进一步解释了应激促进肿瘤发生、影响肿瘤治疗疗效和促进肿瘤生长和转移的机制。
应激与应激反应
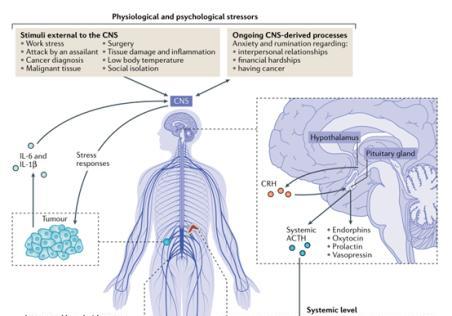
Hans Selye在1956年将应激描述为身体对外界要求的一种反应,以试图恢复体内平衡。为了满足生活需求,从日常事务到肿瘤诊断和治疗等重大威胁,需要调动代谢能量来维持必要的生理适应性反应。这些是通过激活交感神经系统(SNS)和下丘脑垂体肾上腺素(HPA)轴来实现的,导致交感神经末梢和肾上腺髓质局部和全身性的分泌肾上腺素能因子(主要是去甲肾上腺素和肾上腺素),肾上腺皮质释放糖皮质激素,以及阿片类物质、催产素和其他压力调节激素的分泌(图1)。
上述应激反应是由中枢神经系统(CNS)在处理各种刺激后发起的,包括对各种条件的生理反应,如组织损伤、低温或者外部刺激(如被攻击者用武器攻击或被告知患有癌症)等。值得注意的是,应激反应对机体可能是有利的,也有可能是有害的;并且不同个体对内部或外部刺激的应激反应强度和持续时间明显不同,这取决于生理因素,包括遗传和发育变异以及身体素质;个体心理社会特征,包括感知到的社会支持、应对能力和其他个人特征;以及之前经历过的有压力的生活事件的特征,包括童年的不幸。由此得出的结论是,诸如肿瘤诊断、治疗和存活等压力因素可能会对不同患者产生不同的体验,从而引发不同的应激反应。因此,应激干预疗法,无论是行为疗法还是药理学疗法,都应该因人而异。
图1应激与肿瘤的相互作用
肿瘤进展的关键时期
正常细胞通过获得具有进化优势的独特特征转化为恶性细胞,即癌症的“特征”。这些特征包括抗凋亡信号、独立于外部生长信号、促血管生成的能力、逃避免疫破坏以及获得具有侵袭性特性进入远处的器官、在允许的微环境中形成转移灶。重要的是,在这一转变过程中,癌前病变或恶性病灶可能被消除,可能成为潜伏或缓慢发展,或可能发展为具有临床表现的病灶。
在上述肿瘤进展的关键时期,应激可能会产生重要的影响。应激是否会加剧或减轻恶性过程可能取决于恶性进展的阶段、特定的肿瘤特征以及应激反应的特征。此外,免疫系统与肿瘤的相互作用可能抑制或促进肿瘤的生长,而应激相关激素可以同时调节上述这两个过程。因此,应激和癌症之间的相互作用被认为是非线性的,应激对肿瘤的作用可能取决于癌症进展的阶段。在临床实践中,上述肿瘤进展潜在的关键时期很难被准确的界定,特别是关乎到肿瘤预后的治疗过程,这也许是实践中应激对肿瘤作用被削减的重要原因。
应激影响肿瘤的机制
正如大量文献证实的那样,应激可以通过调节肿瘤的大多数特征来促进肿瘤的进展,并且此作用的分子和系统机制已经被阐明。本综述主要从肿瘤起始阶段以及肿瘤进展阶段加以阐述。
一、肿瘤发生阶段
1、DNA损伤
特定的应激因素已被证明会导致DNA损伤并危及DNA修复,从而潜在地促进细胞的恶性转化。特别是,在小鼠成纤维细胞系中,来自应激小鼠的血清,或肾上腺素、去甲肾上腺素和皮质醇(每种因素单独作用或联合时协同作用),增加了紫外线照射后的细胞DNA损伤和/或减少了DNA修复。在小鼠和人类非癌细胞系中,β-肾上腺素能受体(β-AR)介导的活性氧生成和β-抑制素MDM2依赖的p53降解增加了DNA损伤并抑制了DNA修复。相应的体内研究也证实,糖皮质激素介导的应激反应也可导致MDM2依赖性p53下调,并增加电离辐射后的细胞抗凋亡特性。在人体中,几项研究表明,心理压力与DNA损伤的增加相关或有因果关系,一些人类癌细胞在体外随着β-肾上腺素能和糖皮质激素信号的传递而表现出加速的DNA损伤,部分是通过ATR p21通路激活的。
2、致癌病毒
13-15%的人类癌症发病可归因于致癌感染,应激也可通过促进致癌病毒的流行和爆发从而增加癌症发病的风险。在体外感染各种人类细胞系后,主要的致癌病毒可被糖皮质激素或儿茶酚胺重新激活,包括人乳头瘤病毒(HPV)、EB病毒、卡波西肉瘤相关疱疹病毒以及乙型和丙型肝炎病毒。此外,应激激素在感染致癌病毒的人类细胞中刺激致癌基因表达,并抑制白细胞中I型干扰素(IFN-α和IFN-β)的表达,损害抗病毒免疫能力。
3、肿瘤发生
多项动物试验评估了应激对实际肿瘤发生的影响,而不是对中间指标的影响,如DNA损伤或致癌病毒的活化等。重复束缚应激,社会隔离和寒冷的环境温度促进致癌物诱导的肿瘤发生。在自发性癌症的转基因模型中,重复束缚应激通过β2-AR信号促进了胰腺癌的发生,而去交感神经化抑制了前列腺癌的发生。然而,在这些加速诱导癌症的模型中,很难区分应激对肿瘤的作用是在发生阶段还是在进展阶段,因为应激的时间进程在很大程度上既与发生阶段也与发展阶段重叠。因此目前认为,应激可能会加剧致癌物质暴露对机体的影响,但在没有已知接触致癌物质的情况下,还不清楚应激是否是促进肿瘤发生的重要因素。
二、肿瘤进展阶段
1、对肿瘤细胞的作用
交感神经末梢、免疫细胞或肿瘤细胞在肿瘤微环境中分泌或局部释放应激激素,可直接影响肿瘤细胞,促进其恶性特性。具体来说,去甲肾上腺素和肾上腺素在体外可以促进肿瘤细胞的增殖、存活(抗凋亡)、迁移、侵袭、上皮间充质转化(EMT)以及前列腺素和基质金属蛋白酶(MMPs)的产生(图2)。因此,在动物模型中,行为或生理应激源可以通过激活肿瘤β-AR来促进肿瘤的生长和转移,这些机制已经通过特定的药理学或分子阻断或基因敲除试验得到验证。
最近的研究表明肿瘤神经支配对肿瘤的进展有重要的影响。肿瘤可以分泌神经元生长因子,增加肿瘤的交感神经支配。这就产生了一个前馈循环,在应激诱导的交感神经激活状态下,肿瘤局部去甲肾上腺素水平升高,促进癌症的进展。同时,许多人类癌症被发现β-AR高表达,它们的高表达以及肿瘤局部高浓度的去甲肾上腺素和/或血浆肾上腺素水平与更大的肿瘤体积,更晚的肿瘤分期,淋巴结转移以及生存率降低有关。有趣的是,卵巢癌患者的低社会支持预示着更高的去甲肾上腺素水平。行为应激也可以通过糖皮质激素分泌来促进肿瘤生长,乳腺癌模型中,合成的糖皮质激素受体(GR)激动剂(例如地塞米松)促进肿瘤转移并降低生存率。在乳腺癌患者中,GR和GR调节激酶的表达水平越高,生存率越低。
图2应激对肿瘤以及肿瘤微环境的影响
2、血管及淋巴管生成
体外研究结果表明,去甲肾上腺素和肾上腺素可促进肿瘤细胞多种血管生成因子的表达和分泌,包括血管内皮生长因子(VEGF)、白细胞介素-6 (IL-6)和IL-8,而在肿瘤细胞与内皮细胞直接接触后,去甲肾上腺素介导的血管生成得到加强。在原位植入人卵巢癌细胞的应激裸鼠中,β2-AR/cAMP/蛋白激酶A (PKA)信号传导可增加肿瘤VEGF的表达、肿瘤血管化和生长。在胰腺癌、结直肠癌(CRC)和乳腺癌模型中也证实了类似的发现。应激诱导的β-AR信号通路也通过表观遗传调节抑制前列腺癌异种移植物中抗血管生成因子血栓反应蛋白1 (thrombospondin 1, TSP1)的表达从而促进肿瘤进展。在卵巢癌患者中,较低的社会幸福感和较高的抑郁症状与较高的血浆和肿瘤VEGF水平以及较高的腹水和血浆IL-6水平相关。
3、免疫调节与炎症
应激已被证明会促进炎症和免疫逃避。大多数免疫细胞表达β-ARs、前列腺素受体和GRs,应激对其活性和分布的影响已在动物模型和癌症患者中得到广泛的研究。在小鼠模型中,自然杀伤细胞对肿瘤细胞的杀伤能力被应激诱导的β-肾上腺素能信号或β-肾上腺素能激动剂抑制,并且应激诱导的肺转移的增加也被证明是通过抑制自然杀伤细胞介导的。在CRC和鳞状细胞癌的小鼠模型中,应激还能诱导T辅助1细胞(TH1细胞)类型向T辅助2细胞(TH2细胞)类型细胞因子产生的转变,从而促进肿瘤的生长。关于炎症,在临床前研究中,应激诱导的β-肾上腺素能信号传导被证明可促进肿瘤细胞和肿瘤相关巨噬细胞(TAMs)中COX2的表达和前列腺素的分泌,进而刺激促炎细胞因子(如IL-6)的分泌,促进肿瘤局部对巨噬细胞的募集及其向M2的极化,最终促进肿瘤的进展。
4、肿瘤转移
肿瘤的转移受多种机制调控。例如,在小鼠中,应激诱导的β-AR激活通过上调骨髓干细胞(BMSCs)中核因子κB受体激活因子配体(RANKL)的表达,促进循环肿瘤细胞向骨骼迁移。还可以通过CC-趋化因子配体2 (CCL2) CC-趋化因子受体2 (CCR2)介导巨噬细胞的迁移,从而形成转移前生态位,增加器官特异性转移。此外,应激增加肿瘤细胞EMT,促进肿瘤和基质细胞分泌MMPs和肿瘤细胞的抗凋亡,进而促进恶性细胞脱离,转移和在循环中存活。在乳腺癌和卵巢癌患者中,感知到的压力、抑郁症状或社会孤立预示着更高的肿瘤EMT相关基因的表达,以及肿瘤细胞和/或TAMs中更高的MMP9水平。重要的是,β-AR阻断在许多小鼠模型中减少了应激诱导的转移,包括实验性转移和自发性转移。同时,在胃癌和肺癌患者中,肿瘤β-AR表达水平与淋巴结转移相关,而β-阻断剂的使用与乳腺癌和卵巢癌患者的转移或复发减少相关,并与黑色素瘤和乳腺癌的生存率提高相关,但肺癌和卵巢癌的生存率没有提高。考虑到不同肿瘤的结果不一致,因此未来需要更多的RCT试验来验证β-AR阻断剂对癌症的长期影响。
流行病学研究
一项对2008年发表的142项前瞻性研究(每项研究的平均样本量为87,000人)进行的meta分析表明,心理社会应激预测癌症发病率将增加6%(OR=1.06;95% CI 1.02-1.11, p=0.005)。值得注意的是,抑郁是造成这种影响的主要因素,而不是压力生活事件。然而,meta分析发现了一个显著的发表偏倚,被纳入研究的结果存在显著的异质性,76%的研究报告为没有影响, 18%表明有害影响,6%表示有保护作用。最近的一些研究将各种特定的压力因素,包括寒冷的气候、丧亲之痛、战争和抑郁,与各种癌症的高发病率联系起来,但有些研究结果却提示没有任何影响。将工作压力作为一种风险因素,两项荟萃分析得出了不一致的结论:第一项报告了前瞻性研究的零效应,而第二项报告了相对风险的升高(肺癌和CRC分别为1.24和1.36),但后者也包括了容易发生偏差的病例对照研究。
肿瘤患者的应激管理
在人类中测试压力是否影响癌症进展的最可靠的方法是随机对照试验(RCT研究),其中干预是一种经过验证的压力管理方法,观察指标包括心理指标、中期生物标志物,以及最重要的是,癌症长期预后。这种随机对照试验对于研究癌症发病率并不实用,但对于研究癌症进展和死亡率是可行的。过去40年里,进行了多项心理和药理随机对照试验,例如最近的meta分析累计确定了22项采用心理社会干预的随机对照试验,这些试验采用了Cochrane或其他标准,在方法上是严格的。大多数干预至少在术后一个月开始(16/22随机对照试验)和/或在转移性疾病患者中进行(12/22RCT);大多数研究采用的是群体干预(14/22 RCT),而不是个体干预(7/22 RCT)。重要的是,大多数干预措施确实改善了心理指标,也改善了一些生理生物标志物(例如,自然杀伤细胞活性)。综合这些meta分析和作者对这22项研究的评估,没有明确的证据表明心理干预在肿瘤长期预后方面有改善,但该结果仍然是有价值的。具体来说,即一些干预措施可以在干预后的最初几年里延缓疾病的进展,但在这一初始阶段之后,效果就不那么明显或根本就没有。心理社会干预可能有暂时的效果,因为它们对肿瘤生物学的影响是短暂的,或者因为患者对心理干预的依从性在随访期间呈逐渐减少的趋势。但是有人指出,一些特殊患者可能比其他患者更能从心理干预中获益,特别是老年、未婚、心理脆弱或压力大的患者,以及处于疾病早期阶段的患者(例如,早期黑色素瘤)。近些年来,一些RCT试验使用了药物干预来拮抗癌症患者的应激反应,所有这些试验都使用了非选择性β-阻断剂普萘洛尔,选择该药物的最重要的原因是基于其在动物模型中的有效的抗肿瘤作用以及其相对于其他肾上腺素能拮抗剂的高安全性。
结论与展望
尽管应激促进癌症的发生尚未达成共识,但已有确凿的证据表明应激可通过调控癌症的大多数特性促进其进展。动物研究已证实介导这一效应的分子和系统机制,其中大多数在癌症患者中得到了证实。交感神经系统引起的肾上腺素能应激反应以及医疗程序中的肾上腺素能炎症反应是应激有害影响的关键介质。在一些模型中,合成类固醇的使用和应激诱导的糖皮质激素释放也被证明促进了癌症的进展,降低了辅助治疗的疗效。然而,需要注意的是,动物研究可利用其优势将应激同步暴露于癌症生长和转移易受应激影响的特殊阶段。相反,流行病学研究和大多数临床试验评估应激-减轻心理干预并不聚焦于癌症的应激敏感阶段,亦有一些在临床中不易被识别和解决。故流行病学研究和临床干预研究显示出效果小或结果复杂也就不足为奇了。重要的是,心理干预有可能对病人的应激反应进行个体化处理,可能产生持久的治疗效应,而没有药物不良反应,对有药物治疗禁忌的患者是可行的。基于我们目前对癌症生物学、应激以及在癌症连续体中关键时间框架内它们之间复杂的相互作用的理解,我们假设应激管理干预可以降低癌症复发和死亡率,尤其是在接受治疗性肿瘤手术的患者中。为促进这种有益的效果,我们建议在影响癌症进展的关键时期,特别是短暂的围手术期和辅助治疗期间,进行应激管理干预措施的验证,并与其他时期进行比较;应同时采取药理学方法,克服医疗程序不可避免地引发的应激和炎症反应;并应包括个性化模块,以适应患者的独特特点和需求,并重点关注应激症状表现明显的患者。这样的研究应该类似于测试一种新的药物疗法,并且可能需要非盈利资助组织的优先考虑。近期的生物标志物临床试验,包括药物缓解压力的干预措施,提示这种方法具有降低癌症死亡率的潜能。基于目前的数据,我们认为这些方法应该通过大型合作的多中心RCT进行测试,评估统一干预对长期癌症预后的影响,其严格程度应类似于研究新的癌症治疗药物。
“论肿道麻”述评
近年来,应激一直被认为是影响癌症发生发展的因素之一。但应激与癌症的联系在动物研究和临床研究中并未形成共识。本文总结了目前的循证医学证据,阐述了应激和癌症之间的联系。提示目前已有确凿的证据表明应激可通过调控癌症的大多数特性促进其进展。尤其是从动物研究中已经证实应激可以通过调节癌症发生的相关因子的变化来促进癌症的发展,对癌症发展中肿瘤微环境的形成有着促进的作用,并且已经明确了导致这些改变的分子机制,且大多数已在患者身上体现。其中交感神经系统引起的肾上腺素能应激反应和伴随医疗过程的肾上腺素能炎性反应是应激产生有害作用的关键环节。另外,合成类固醇的使用和应激引起的糖皮质激素释放可促进癌症的进展,降低辅助治疗的疗效。然而,需要注意的是,动物研究可利用其优势将应激同步暴露于癌症生长和转移易受应激影响的特殊阶段。相反,流行病学研究和大多数临床试验评估应激-减轻心理干预并不聚焦于癌症的应激敏感阶段。故流行病学研究和临床干预研究显示出效果小或结果复杂也就不足为奇了。重要的是,心理干预有潜力对病人的应激反应进行个体化处理,可展现出持久的治疗效应,且无药物副作用,其对存在药物禁忌症的患者尤为适用。
基于目前对癌症生物学、应激以及它们之间复杂的相互作用,使用应激管理干预可以降低癌症的复发和死亡率,尤其是在接受治疗性肿瘤手术的患者中。为促进这种有益的效果,作者建议在影响癌症进展的关键时期,特别是短暂的围手术期和辅助治疗期间,进行应激管理干预措施的验证,并与其他时期进行比较;同时采取药物治疗,克服医疗程序不可避免地引发的应激和炎症反应;并应包括个性化调控,以适应患者的独特特点和需求,并重点关注应激症状表现明显的患者。近期的生物标志物临床试验,包括药物缓解应激的干预措施,提示这种方法具有降低癌症死亡率的潜能。基于目前的数据,有必要进行大型合作的RCT进行评估统一干预对长期癌症预后的影响,其严格程度应类似于研究新的癌症治疗药物。因此,在未来数年,随着应激管理干预研究的的开展,这方面的知识有望得到有力的推广,这必将为未来的癌症患者带来福音。
编译:高玲玲,述评:杨礼
审校:张军,缪长虹
参考文献: Stressand cancer: mechanisms, significance and future directions. Eckerling A, Ricon-BeckerI, Sorski L, et al. Nat Rev Cancer. 2021 Sep;21(12):767-785. doi: 10.1038/s41568-021-00395-5.Epub 2021 Sep 10.
声明:古麻今醉公众号为舒医汇旗下,古麻今醉公众号所发表内容之知识产权为舒医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。
不感兴趣
看过了
取消

人点赞

人收藏

打赏
不感兴趣
看过了
取消






您已认证成功,可享专属会员优惠,买1年送3个月!
开通会员,资料、课程、直播、报告等海量内容免费看!

打赏金额
认可我就打赏我~
1元 5元 10元 20元 50元 其它
打赏作者
认可我就打赏我~
扫描二维码
立即打赏给Ta吧!
温馨提示:仅支持微信支付!
已收到您的咨询诉求 我们会尽快联系您
