从“纸上”到“云上”,大数据重构真实世界医学研究体系
优质的临床数据集是RWE(真实世界证据)临床价值体现的前提。
2016年12月,美国颁布《21世纪治疗法案》,要求FDA在医疗产品审批和监管程序中纳入真实世界证据。此事件以来,国内相关具体指南及指导原则也随之陆续发布和执行。随着国家药监局以及海南博鳌乐城利用真实世界数据在器械和新药等多个项目审批的受理,依托真实世界证据解决临床问题的制药企业如雨后春笋般涌现,队伍逐渐扩大。政策导向的持续发力,国内制药领域创新能力与国际竞争力逐步提升,真实世界研究也随之迈入了一个崭新的时代。
从“数据”到“证据”
4月15日,国家药品监督管理局药品审评中心发布《用于产生真实世界证据的真实世界数据指导原则(试行)》,该指导原则首次全面定义真实世界数据及其来源、适用性评价、数据治理、数据合规性、数据安全性以及数据质量管理体系等内容。在此之前,各国组织和机构对于真实世界数据的定义描述各不相同,此次指导原则的颁布进一步为真实世界研究奠定指导性地基。因此,编者对于真实世界研究、真实世界数据以及真实世界证据三者之间的关系做简要梳理:
真实世界数据(Real World Data,RWD)即来源于真实世界环境下所收集到的与研究对象健康状况及诊疗相关的数据。RWD涉及范围包括生理指标、诊疗情况、既往病史甚至生活习惯,其主旨在于把控来自真实医疗环境可反映实际诊疗过程及结果的患者健康状态和疾病转归情况,从而一定程度上减少了对研究对象的选择、干预和对照。
表1 常见的真实世界数据类型
(来源:《重新认识真实世界研究》,CNKI,万联证券研究所)
而真实世界证据(Real World Evidence,RWE)则是根植于对真实世界数据的研究,从而得出在真实环境下干预措施的疗效、长期用药的安全性、依从性、疾病负担等证据。RWE可直接表征在实际使用情况下医疗产品对研究对象群体的临床获益和风险,其意义在于为药品加速审批和安全性验证方面提供重要补充及参考方向。
总而言之,始于收集RWD,止于产生RWE的整个研究过程则被统称为真实世界研究(Real World Study,RWS)。其核心在于针对预设的临床问题,能够补充对医疗真实情况的反映,在辅助临床决策和证明药械的临床价值上提供可行性保障。
真实世界研究全球态势
根据Clinical Trials官网数据显示,血管疾病、心脏疾病、精神障碍、精神分裂、呼吸性疾病以及免疫系统疾病六类疾病为真实世界研究的热门学科。截至2021年5月31日,全球已完成的真实世界研究项目共1013个,其中欧洲国家、美国、中国为主流研究国家及地区。目前除已完成项目之外,仍有约千余项真实世界研究处于正在招募等活跃状态。
表2 全球真实世界研究主要疾病种类及项目数量(已完成)
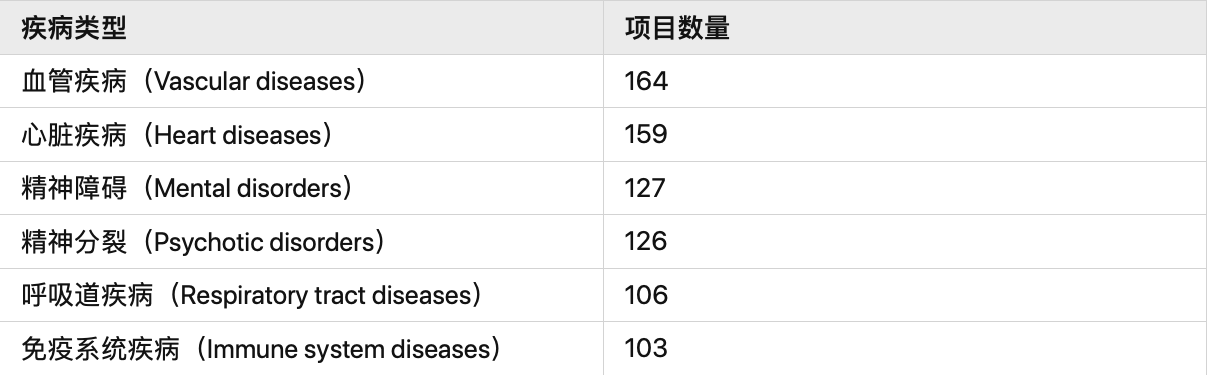
(来源:Clinical Trials.gov,数据更新至2021年5月31日)
为顺应全球发展趋势,国内对于真实世界研究的体系建设和学术研究建设已经初见雏形。 作为研究者们在临床证据的挖掘过程中使用的新方法,有关部门已逐步开放建立科学、可行的研究设计、数据处理分析等方向的技术规范,我国真实世界研究产业已在药械产品全周期管理中成为不可或缺的一环。
大数据科研解决方案助力真实世界研究
真实世界研究过程大致分为以下六个阶段: 确认临床问题、制定研究方案、收集RWD、数据治理、数据统计和分析、结果解读和评价 。RWD是整个研究过程的关键环节,优质的临床数据集是RWE临床价值体现的前提。若无对RWD合理化的解读和分析,RWE的规范化更是无从谈起。
真实世界研究整体过程(来源:动脉网)
在确认临床问题阶段,首先要从根本出发,就长期积累下来的医疗大数据挖掘契合实际临床需求,结合医生在诊疗过程中遇到的“卡脖子”难点,最终确认临床问题。在这样的情况下,基于有价值的临床问题,后期才能为实现RWE支持药品审批决策的目标提供了一个相对清晰的路线图。
在收集RWD阶段,如何打造高效且高质量的数据集成为至关重要的痛点。若数据维度可实现高度结构化,研究者可实现实时监控研究对象数据质量,质量欠佳的数据条目可实现及时解决,那么后续的数据治理过程将变得更加明朗。恰巧,大数据科研解决方案就是一种可达到以上效果的数据收集方法,依托此方法收集到的高质量临床数据更能准确贴合临床端的需求。
在数据治理阶段,数据的预处理、缺失数据的处理、数据集合构建等都是该阶段的重要步骤。该阶段也是实际临床途径直接获取的数据达到可应用于真实世界研究标准的必经之路,同时也是保证RWE能否顺利应用的首要条件。
在数据统计与分析阶段,高效率处理大规模数据和挖掘数据与患者结果的相关性是最终抵达目标的关键。作为从RWD中挖掘RWE的关键步骤,合理的解读与分析最终得出的RWE才能更好的赋能临床。由于RWD的数据量级和复杂程度,人工智能可通过深度学习对已有数据进行全面观测,从而助力RWE的规范化和合理的应用。
医学同样讲究以证据说话,有理可依、有据可循这一准则更是普适于医学研究中。临床端的医生和患者对诊疗解决方案提出了越来越高的要求,因此对真实世界证据的需求则更加迫切。当医学研究携手大数据,或能为医疗体系完善提供全新思路。
【参考资料】
1. 2020年5月,万联证券,《医药生物行业真实世界证据:医学研究体系的重要一环》
2. 2021年4月,蛋壳研究院,《2021真实世界研究行业报告——监管落地,从药品到器械全面应用》
不感兴趣
看过了
取消

人点赞

人收藏

打赏
不感兴趣
看过了
取消


















 010-82736610
010-82736610
 股票代码: 872612
股票代码: 872612
 京公网安备 11010802020745号
京公网安备 11010802020745号










