真实世界数据应用的现实世界突围
☆ 信息孤岛、数据质量不高,是真实世界数据应用的两大难题。
☆ 陈平雁教授认为,要突破数据的制约,自下而上的策略更为可行。
☆ 真实世界数据应用试点是海南推进自由贸易港建设的一项重大制度创新。
随着近年来一系列改革措施的推进落实,新药研发快速发展,同时对药物研发工作的质量和效率也提出了更高的要求。随机对照临床试验(RCT)虽是金标准,但在很多情况下有一定局限性,如何利用真实世界证据评价药物的有效性和安全性,弥补RCTs的局限之处,成为国内外药物研发和监管决策中日益关注的热点问题。
经过一年多的起草和征求意见,今年1月,国家药监局发布了《真实世界证据支持药物研发与审评的指导原则(试行)》;8月,发布了《用于产生真实世界证据的真实世界数据指导原则(征求意见稿)》;9月,又发布了《真实世界研究支持儿童药物研发与审评的技术指导原则(试行)》。
真实世界研究的政策春天看似到来了,但要将其实际应用在研发和监管环节中,能够成为真实世界证据的真实世界数据会有多少?其中的痛点与难点要如何突破?
很多情况下,拿不到数据
数据不可及,是实际面临的第一个难题。
日前,在中欧校友医疗健康产业协会(CAHA)数字医疗专委会“一颗药的数字化旅程”专题研讨会上,中华预防医学会生物统计分会主任委员陈平雁教授表示:当前各家医院对HIS系统的投入都非常大,也积累了海量的电子病历数据,但遗憾的是,这样的真实世界数据缺乏共享机制,成为了信息孤岛,使得真实世界数据的可及性大大降低。
适用数据比例低
虽然有海量数据,但由于数据质量不高,能够潜在产生真实世界证据的真实世界数据的比例很低,是实际面临的第二个难题。
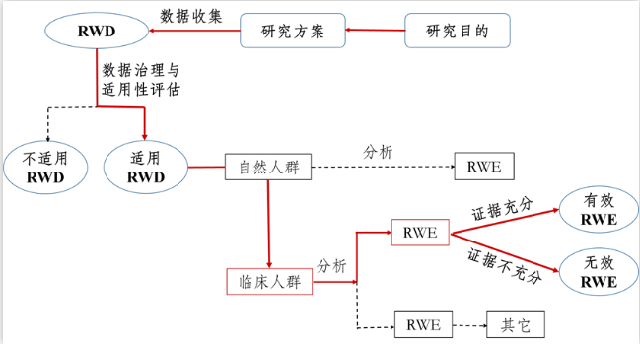
支持药物监管决策的真实世界研究路径(实线所示)
真实世界数据(RWD)指来源于日常所收集的各种与患者健康状况和/或诊疗及保健有关的数据;真实世界证据(RWE)指通过对适用的真实世界数据进行恰当和充分的分析所获得的关于药物的使用情况和潜在获益-风险的临床证据。并非所有的真实世界数据经分析后都能成为真实世界证据,关键的一点是要满足适用性。
适用性主要通过数据的相关性和可靠性进行评估。相关性是评估真实世界数据是否与所关注的临床问题密切相关;可靠性则从数据的完整性、准确性、透明性和质量保证方面进行评价。
陈平雁教授表示:众所周知,我们国家医生承担的工作压力很大,完成每天的接诊量之外,难有精力保证病历的质量,这就导致我们的数据质量普遍不高,能够满足科研要求的数据比例很低。虽然发达国家也面临这个问题,但他们的可用数据比例能达到70%。此外,各单位数据标准不统一也是适用数据不足的重要原因。
如何破局
在数据共享方面,目前乃至将来一段时间内都很难出现根本性的改观。陈平雁教授认为,要突破数据的制约,自下而上的策略更为可行,这需要一线的从业者充分利用数字技术,先围绕自己的产品制定目标,前瞻性地建立自己的对策。
零氪科技CEO张天泽表示:提升数据质量是重点,如果只是数量多但质量不高,那只会徒增存储和处理的成本。比如,临床病历经过数据提取、数据清洗、数据转化以及质量控制等多个治理环节后,最终产生能够用以指导对药物或器械的评估、支持研发和监管决策的真实世界数据,这种高质量的数据才是有价值的。
而要提升数据质量,记录患者就诊和随访等状况的“原件”的保留是重要的第一步,有了这些高质量的“源数据”,才能在此基础上做质量治理,产生用于临床科研、药物研发及监管审批的数据。现在已经有越来越多医院,尤其是科研任务较重的教学性医院,愈发重视高质量、有科研价值的病例数据的产出,所以通常也会要求医生在完成病历书写的时候,尽可能地接近科研级的标准。
“此外,如互联网医院数据等院外的数据也能够为真实世界研究提供支持。可以看到,目前互联网医院在客观上有大量的资本推动,所以在诊疗环节的数字化进程非常快。如何将院外数据与院内数据拼接起来,形成适用于支持科研的真实世界数据,这是目前监管部门以及行业非常关注的。”张天泽说。
试点先行
真实世界数据应用试点是海南推进自由贸易港建设的一项重大制度创新。
2018年,国务院赋予海南省全国唯一的临床急需进口医疗器械和药品(不含疫苗)的审批权,允许在博鳌乐城国际医疗旅游先行区使用国外已经上市、国内尚未注册的创新药械产品。众多肿瘤创新药及罕见病药物随之落户海南,这在满足国内患者就医用药的同时,也产生了许多宝贵的真实世界数据。2019年6月,国家药监局与海南省政府联合启动了海南临床真实世界数据应用试点工作,随后于9月联合发布《先行区临床真实世界数据应用试点工作方案》。这一举措吸引了诸多创新药械厂商,艾尔建的青光眼引流管也成为第一批入选真实世界研究的产品之一。
今年3月,艾尔建的青光眼引流管成为我国首个使用境内真实世界数据获批上市的医疗器械产品,其在注册中使用了在海南博鳌乐城先行区收集的临床真实世界证据进行人种差异评价。该产品的获批为今后真实世界证据在医疗器械注册审批中的应用起到了先行先试的示范作用,也让大家看到海南试点的初步成效。
随后,有47款进口医疗器械产品申报在乐城先行区开展第二批真实世界临床数据研究,比第一批增长292%。这些产品来自30家大型跨国药企,包括波士顿科学、罗氏诊断、领先仿生、捷迈、参天制药、优时比等。
目前,海南真实世界数据应用试点取得的成效仅体现在医疗器械领域,在药品上的应用仍然任重道远。

人点赞

人收藏

打赏














 010-82736610
010-82736610
 股票代码: 872612
股票代码: 872612
 京公网安备 11010802020745号
京公网安备 11010802020745号










