最新CSCO甲状腺癌指南更新要点 一文全掌握!
医学界肿瘤频道Cloudy
临床上甲状腺癌按病理分型分为:乳头状癌、滤泡癌、髓样癌和未分化癌。其中乳头状癌和滤泡癌合称为分化型甲状腺癌(DTC)。
分化型甲状腺癌的一线治疗措施包括手术、131I、促甲状腺激素(TSH)抑制治疗。但目前国内外的最新研究数据表明,DTC经一线治疗后,其持续或复发率为14.9%,转移率为7%-23%。
本文将更新要点梳理如下。
诊断部分的更新要点
prm-DTC诊断MDT模式
持续/复发及转移性甲状腺癌的诊断应采用多学科协作(MDT)模式;
MDT原则应该贯穿每一位患者的治疗全程;
MDT:超声科、放射科、病理科、外科、核医学科、内分泌科、放疗科、肿瘤科等。
prm-DTC血清学诊断
实验室检查
I级推荐:血清甲状腺球蛋白(Tg)、甲状腺球蛋白抗体(TgAb)及TSH(2A);
II级推荐:穿刺洗脱液Tg测定(2A)。
Tg监测有助于DTC术后病情评估及复发风险分层;
在全甲状腺切除后,无TgAb干扰时,低血清Tg水平具有较高的阴性预测值;但是,由于受残余甲状腺组织、血清TSH及TgAb水平等因素的影响,目前尚无明确的最佳界值点用以指导131I治疗决策。
prm-DTC病理检查

PTC:乳头状甲状腺癌;FTC:滤泡状甲状腺癌
新增需参照2017年新版WHO甲状腺肿瘤分类明确组织学类型;
新增FTC,需尽可能评估血管内癌栓数量。

BRAF启动子与TERT共突变与PTC侵袭性、复发、死亡风险与发生碘难治 等密切相关;
除外 BRAFV600E,新增预后不良标记TERT启动子、TP53。
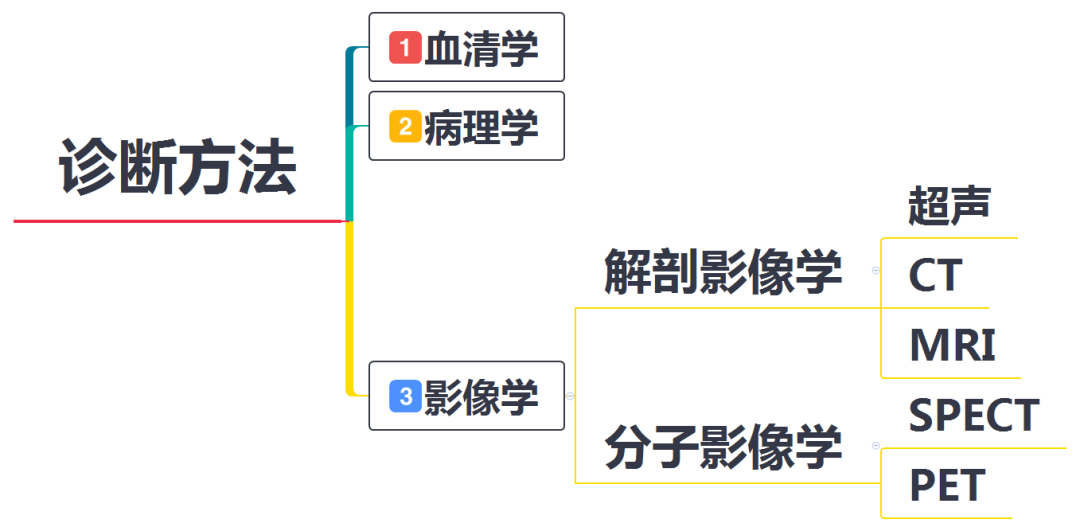
prm-DTC影像学诊断

■超声适用情况
评估内容:
包括颈部淋巴结、甲状腺床、颈部软组织、 血管、气管、食管部分良性病变(术后癜痕、缝线肉芽肿、食管气管憩室、断端神经瘤以及炎性反应增生性淋巴结等)和复发病灶鉴别困难。
正确解释需结合临床病史和血清学检查结果。
■颈部增强CT或MRI适用情况
评估超声无法完全探及的部位(纵隔和区淋巴结,或者Tg+/Us-) (Ⅱ级推荐);
评估复发病灶或淋巴结与周围结构及器官的相对关系(如气管、食管、颈动脉鞘),为手术范围提供帮助 (Ⅱ级推荐);
神经系统以外转移(Ⅱ级推荐);
怀疑脑转移的影像常规检查项目(I级推荐)。
■prm-DTC放射性碘扫描适用情况
局部病变Ⅱ级推荐,远处转移I级推荐。
放射性碘扫描分类及作用:
131I-全身现象(WBS)评估病灶的摄碘能力,判断疗效;
131I-SPECT/CT协助摄碘灶定位和定性,辅助治疗决策。
■ prm-DTC其他影像学检查
18F-FDG-PET/CT(Ⅱ级推荐):适用于131I消融后,Tg或TgAb持续升高,其他影像学检查阴性时;
内窥镜(I级推荐):适用于怀疑气管、食管受累时。
化疗与靶向治疗更新要点
化疗
无症状、稳定或缓慢进展:I级推荐为定期随访(2A);
有症状或进行性RAIR-DT:Ⅲ级推荐为阿霉素(2B)。
分子靶向治疗
无症状、稳定或缓慢进展:I级推荐为定期随访(2A);
有症状或进行性RAIR-DT:
I级推荐:索拉非尼(1A);
Ⅱ级推荐:仑伐替尼(1B);
Ⅲ级推荐:参加临床试验(2B)。
不良反应及处理策略
■ 治疗开始前
基线危险因素评估与干预
全面评估患者是否存在某些可能导致靶向治疗不良反应发生风险升高的危险因素,权衡治疗利弊,确立个体化的治疗方案。
控制合并症。
患者教育
对患者进行潜在不良反应教育,告知患者需及时就诊的临床表现;
患者心理教育。
■ 治疗过程中
密切的患者监测和处理
NCI-CTCAE标准评估;
密切监测患者并提供快速且有效的支持措施,
以将不良反应的风险及严重程度降至最低。
不良反应管理
MDT模式下积极处理复杂不良反应;
依据不良反应,考虑剂量调整或中断。
外照射治疗更新要点
治疗选择更新
强调转移性肿瘤局部治疗的重要性:局部控制与生存相关,转移性肿瘤无病生存可转化为生存获益;
特別强调针对寡转移的局部区域治疗:寡转移的局部治疗可改善寡转移患者的生存;
转移性肿瘤大分割照射+免疫治疗:大分割照射可增加肿瘤免疫原性,利于放疗与免疫治疗的联合。
局部持续/复发病灶:Ⅱ级推荐为外照射(不可切除或碘难治病灶)(2A)
转移性病灶:
肺转移:Ⅱ级推荐为外照射(寡转移)(2A);
Ⅲ级推荐为外照射(多发转移,局部转移病灶危及生命或伴有严重压迫等症状者)(2B)。
骨转移:Ⅱ级推荐为外照射(有症状或承重骨)(2A)。
脑转移:I级推荐为外照射(寡转移)(2A);
Ⅱ级推荐为外照射(多发转移)(2B)。
外放射治疗更新细节
寡转移定义更改:寡转移目前没有统一定义标准通常认为转移灶在1-5个以内;
肺转移适应证补充“局部转移病灶危及生命或伴有严重压迫等症状者”的描述;
取消具体剂量推荐,更改为“大分割治疗有明显的生物学和经济学优势,与新型治疗手段联合可能有潜在临床获益,尚需进一步研究证实”;
指南将“三维外照射技术”更改为“三维或调强外照射等技术。
外科治疗更新要点
■ 外科治疗的总原则中增加并强调:
手术时机的选择和手术范围的确定是外科医生在诊治这类患者时需要重点考虑的问题;
外科治疗的目标是尽可能治愈或控制疾病、改善生存并保留重要器官的功能;
手术次数对预后有明显影响,三次以上手术的患者预后更差。
■ 在手术治疗前专科评估中强调:
结构性病灶是再次手术的靶病灶,因此对外科医生来说,术前影像学检查是最重要的评估内容,需明确是否存在结构性病灶并定位病灶;
无周围重要结构侵犯的局部持续/复发及转移病灶的外科治疗策略 调整后的颈侧区淋巴结清扫范围一般包括ⅡⅢ、Ⅳ、V区或其中1-2个区域;
■ 病灶侵犯周围重要结构的局部持续/复发及转移病灶的外科治疗策略:
突出病灶可能广泛侵犯的特征:粘连、侵犯周围的重要结构,如喉、气管、食管、颈血管和重要的神经,如喉返神经、迷走神经、交感神经、膈神经、臂丛神经等;
在注释中增加了切除后修复重建的方法:对于侵犯到气管腔内的病灶,常采用节段性切除、端端吻合方法重建气道,不能端端吻合者可采用自体血管化皮瓣及肌皮瓣方法修复气道;
在病灶侵犯至食管腔内的患者中,切除大范围侵犯的病灶后亦需重建修复食道,可采用自体血管化皮艦及肌皮瓣方法进行修复,切除局部侵犯的病灶后可直接对位缝合修补管腔;当病灶仅侵至食道肌层时,通常可在黏膜下解剖、切除病灶,不需要食道重建。
■ 强调术前专科情况评估(I级推荐为主):
①既往术式范围
②手术并发症/证据
血钙/PTH;
喉镜检查声带情况。
③病理结果/疾病分期
④结构性病灶存在的客观依据
基本指标:Tg/TgAb+超声;
重要方法:颈胸部增强CT。
⑤其它考虑
年龄
疾病播散程度(全身/局部)
合并症
■ 无重要结构侵犯病灶的外科治疗策略 (Ⅱ级推荐为主):
①中央区病灶
最小径<8mm时,密切随访;
最小径≥8mm时,再次手术;
术前穿刺证实转移;
再次手术时补充全甲状腺切除术,并进行规范的区域淋巴结清扫术。
②侧颈区病灶
最小径<10mm时,密切随访;
最小径≥10mm时,再次手术;
术前穿刺证实转移;
前次未发现病灶的侧颈区:治疗性改良颈侧区淋巴结清扫术,保留关键结构;
前次手术过的侧颈区域病灶:可调整清扫区域使其更为局限(1-2个区域)。
■ 喉返神经受累:
无声带麻痹,尽量切肿瘤、保神经(I级推荐);
明确声带麻痹、肿瘤包裹神经切病灶及受累神经(I级推荐);
尽可能,术中重建神经(Ⅱ级推荐);
■ 气管食道消化道受累(Ⅱ级推荐):
未侵入管腔时,可剔除肿瘤;
侵入管腔内者,切病灶及受累器官,修复重/建造口术;
无法切除、有窒息/明显咯血时,可行局部姑息性手术。
■ 颈血管受累(Ⅱ级推荐):
单侧颈内静脉明显受累可切除受累颈内静脉;
双侧颈内静脉受累,可切除受累血管、至少重建一侧;
颈总动脉局限性受累时,切除后需进行血管重建。
■ 再手术时喉返神经及甲状旁腺的保护:
喉返神经的保护(Ⅱ级推荐):
术中喉返神经监测;
术中发现喉返神经损伤时尽量一期修复;
术后诊断神经损伤者可行手术探查、二期修复。
甲状旁腺的保护(I级推荐):
术中辨识、保留或移植甲状旁腺;
远处转移手术治疗:肺、骨、脑、其他均为Ⅱ级推荐。
内分泌治疗
TSH抑制治疗策略
■ 治疗分类
初治期(I级推荐):
结合TSH抑制治疗副作用风险设定个体化TSH自标(1A);
副作用风险低危:<0.1mU/L(2A);
副作用风险中高危:可耐受的前提下<0.1mU/L—正常下限(2A)。
随访期:
I级推荐:结合患者对治疗反应的动态评估和TSH抑制治疗副作用风险,调整TSH目标(2A)。
Ⅱ级推荐:(1)疗效满意:正常下限-2.0mU/L(2A);(2)疗效不确切:正常下限附近(2A);(3)生化疗效不佳:0.1mU/L-正常下限, 副作用低危时<0.1mU/L(2A);(4)结构性疗效不佳:可耐受的前提<0.1mU/L(2A)。
■ TSH抑制治疗不良反应管理及处理策略(I级推荐)
所有的潜在不良反应:制定合理TSH抑制治疗目标,定期监测治疗副反应,及时调整L-T4用量(1A);
心血管系统不良反应:基础心血管系统状态评估(2A),β受体阻滞剂(2A);
骨骼系统不良反应:基础骨骼系统状态评估(2A),骨质疏松症(OP)初级预防;抗OP治疗(2A)。

